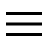Produire de l'énergie propre grâce à l'électrolyse de l'eau ? C'est possible grâce aux électrodes en dioxyde de titane
Il est sur le point de finir écrasé, sa mère le sauveNous connaissons tous le processus deélectrolyse, qui permet de scinder les molécules d'eau en deux sous-produits, deux ions, un H+ positif et un OH- négatif, ce dernier défini comme ion hydroxyle. Le moins simple est de comprendre comment il est possible de produire de l'énergie propre à partir de ce processus. En effet, en stockant de l'hydrogène, il serait possible de produire de l'électricité.
Certains érudits l'ont fait Stanford, qui a réussi à surmonter les limites liées à la corrosion des électrodes, dans un environnement considéré comme hostile, comme celui de l'eau. En attendant, il convient de noter que les électrodes sont généralement en silicium. Ce dernier aide en fait à la production d'électrons mais est facilement éliminé par l'eau.
Pour pallier à cet inconvénient, disons mineur, l'équipe de scientifiques a mis au point une couche protectrice de le dioxyde de titane d'environ deux nanomètres d'épaisseur, capable de garantir aux électrodes la durabilité pour résister à l'eau pendant le processus de fractionnement. De plus, en plus du dioxyde de titane, les chercheurs ont inséré une couche de iridium ultra mince qui agit comme un catalyseur pour l'ensemble du processus.
Ce nouveau système utilise l'énergie solaire pendant la journée pour diviser les molécules d'eau en oxygène et en hydrogène, puis les stocker jusqu'à ce que, une fois l'obscurité tombée et la lumière du soleil disparue, l'hydrogène et l'oxygène puissent à nouveau s'unir pour créer énergie électrique.
L'équipe, dirigée par l'ingénieur Paul McIntyre et le chimiste Christophe Chidsey, a donc conçu une électrode à base de silicium robuste capable de résister à un environnement hautement corrosif, surmontant l'un des défis les plus difficiles posés ces dernières années concernant le processus d'électrolyse. « En théorie, la séparation de l'eau est un moyen propre et efficace de stocker de l'énergie. Malheureusement, résoudre un problème en crée un autre », a déclaré McIntyre. "Les électrodes sont généralement en silicium, un matériau qui se corrode."
D'où le choix de le dioxyde de titane. "Le dioxyde de titane est parfait pour cette application", a expliqué McIntyre sur le site Physorg. "Il est transparent à la lumière et peut être efficace pour transférer l'énergie électrique, tout en protégeant le silicium de la corrosion."